Unterzuckerungen, oft kurz als Hypos bezeichnet sind häufig die Ursache für eine instabile Stoffwechselsituation mit starken Glukoseschwankungen. Sie zeigen sich als Wechsel von zu hohen und zu tiefen Glukosewerten. Selbst milde Hypoglykämien führen bei manchen Patienten zu einer autonomen (vom Organismus ausgehenden) Gegenregulation.
Das ist der Fall, wenn im Organismus körpereigene Glukose vorhanden ist. Diese ist als „Speicherzucker“ (Glykogen) gespeichert in der Leber (ca. 150 g), zum Teil auch in der Niere und in der Muskulatur. Dabei dient vor allem der Speicherzucker in der Leber (Leberglykogen) der Aufrechterhaltung eines stabilen Glukosespiegels.
Weil bei einer Unterzuckerung Glukose ausgeschüttet wird, so kommt es zu einem schnellen und steilen Glukoseanstieg, steiler als er selbst beim Essen von schnell resorbierbaren Kohlenhydraten (wie Traubenzucker, Fruchtsaft, Cola etc.) auftritt. Das ist leicht vorstellbar, denn diese körpereigene (endogene) Glukose kommt sofort in den Blutkreislauf und erreicht diesen nicht erst über den Umweg über den Magen und den Darm. Man kann sich das so vorstellen wie bei einer Sparkasse, welche Geld verleiht.
Hat man keins und benötigt welches, dann nimmt man einen Kredit. Der Körper braucht Glukose, bekommt aber keine von außen, so gibt es Kredit über die Glukose aus der Leber.
Allerdings wissen wir auch, dass Kredite zurückgezahlt werden müssen. So wie die Sparkasse ihr Geld wieder einfordert, möchte die Leber die aus ihren Reserven abgegebene Glukose zurückhaben. Der Körper versucht die nach einer Gegenregulation geleerten Glukosespeicher zu restaurieren, wenn später durch Nahrungsaufnahme wieder externe Glukose verfügbar ist. Dann fließt diese auch in die leeren Speicher (und wird in Speicherzucker umgewandelt), steht in diesem Moment aber nicht für den allgemeinen Verbrauch zur Verfügung.
In den CGM-Profilen zeigt sich dieser Effekt durch eine nur geringe oder gar ganz fehlende Auslenkung der Glukosewerte nach dem Essen, obwohl die Mahlzeit richtig geschätzt und abgedeckt wurde. Dagegen sieht man den nahrungsbedingten höheren Wert, wenn man die Glukose im Blut (also mit einem klassischen Blutglukosemessgerät) misst. Ein repräsentatives Beispiel dazu zeigt Abb.1. Der Betreffende mit Typ-1-Diabetes wies vor dem dargestellten Profil bereits über mehrere Tage immer wieder sich wiederholende Unterzuckerungen auf (mehr > 2 pro Tag), so dass die Zuckerspeicher (Glykogenspeicher) geleert waren. Die CGM-Kurve ist ordnungsgemäß kalibriert worden (dies war bei dem verwendeten CGM-System alle 12 Stunden notwendig).
Es zeigt sich, dass die Einnahme der Mahlzeiten kaum Auslenkungen in der Glukosekurve zur Folge hatte (z.B. gegen 12.00 Uhr, gegen 18.00 Uhr und gegen 22.00 Uhr). Um 18.00 Uhr kommt es sogar zum Abfall der Glukosekurve, obwohl die 7,5 Einheiten Insulin bei 75g Kohlenhydraten richtig dosiert sind. Ursache für diesen Verlauf ist der Fluss von Glukose hauptsächlich zur Leber zwecks Restauration der Zuckerspeicher.
Das gezeigte Verhalten ist als „Pseudonormalisierung“ zu beschreiben: Es entsteht ein flacher, scheinbar normoglykämischer Glukoseverlauf aufgrund des Wechselspiels von sich wiederholenden Hypoglykämien, der Ausschüttung von körpereigener (endogener) Glukose und des Versuchs der Wiederauffüllung der Zuckerspeicher [1]. Ist die Restauration der Speicher unvollständig so besteht dauerhaft die Gefahr einer schweren Folgehypoglykämie.
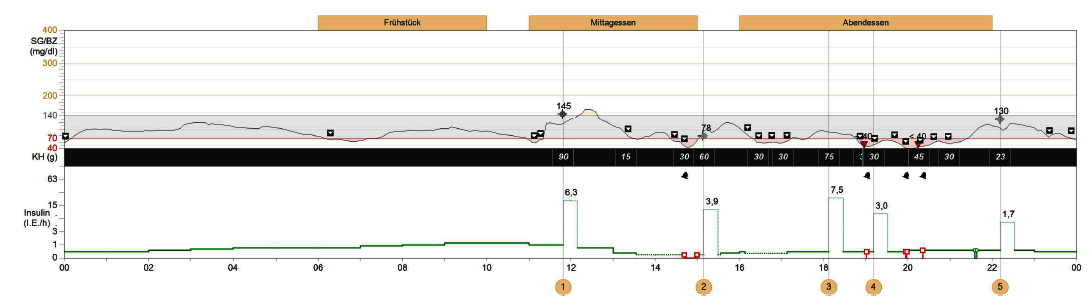
Abb. 1. „Pseudonormalisierung“ als Ausdruck nicht vollständig restaurierter Zuckerspeicher nach wiederholt aufgetretenen Unterzuckerungen. Die Einnahme der Mahlzeiten hatte kaum Auslenkungen in der Glukosekurve zur Folge, da ein Teil der Glukose zur Wiederauffüllung der Zuckerspeicher genutzt wird, folglich nicht am Glukosesensor ankommt, der im Gewebe sitzt.
Der Glukoseanstieg ist vollständig nur im Blut, nicht jedoch im Gewebe sichtbar (zum besseren Verständnis kann man sich noch einmal Abb. 1 aus dem Beitrag vom 13.09.22 in der Blood Sugar Lounge ansehen: „Unterschiede der Messwerte im Blut und im Unterhautfettgewebe (zwischen Blutglukose- und Sensorglukosewerten) – sind CGM-Systeme ungenau?“)
Mitunter führen die Anwender des CGM angesichts solcher Kurven im post-prandialen Zustand (also nach dem Essen) Blutglukosemessungen durch, weil sie den CGM-Daten misstrauen. Dabei sind die Blutglukosewerte in dem beschriebenen Zustand meist deutlich höher als die Glukosewerte im Gewebe (in Abb.1 hatte der CGM-Anwender keine solchen Messungen vorgenommen).
Ein Beispiel dazu zeigt Abb. 2. Nach dem Wechsel des Sensors gegen 12.30 Uhr tritt aufgrund der zum Mittagessen verabreichten Insulinboli zwischen 15.00-18.00 Uhr eine Unterzuckerung auf. Mehrfach unterbricht die Insulinpumpe die Insulinlieferung, was der Anwender quittiert und worauf er mit Fruchtsaft reagiert, richtigerweise, ohne sich einen weiteren Bolus abzurufen.
Als die Werte gegen 18.00 Uhr wieder sinken nimmt er noch einmal Nahrung ohne Insulinabgabe auf, wodurch die Glukosekurve ansteigt. Gegen 19.00 Uhr misst er die Blutglukose und stellt fest, dass die Werte etwas erhöht sind (>180 mg/dl). Er vertraut den niedriger liegenden Sensorwerten nicht und gibt sich einen weiteren Bolus von 15 I.E. Die späteren Essensaufnahmen gegen 19.30 Uhr und gegen 20.00 Uhr hätten die Unterzuckerung vermeiden können, wenn diese nicht wiederum mit Insulin abgedeckt worden wären.
Das Problem war, dass der Anwender sein Insulin entsprechend den erhöhten Blutglukosewerten gegen 19.00 Uhr dosiert hatte. Allerdings lag eine Situation großer Glukosedynamik vor, gekennzeichnet durch den Glukoseabfluss zur Restauration der Zuckerspeicher. In der Situation gegen 19.00 Uhr waren die Blutglukosewerte und die CGM-Werte im Gewebe verschieden, beide jedoch korrekt gemessen jeweils in ihrem Medium (Blut und Gewebe).
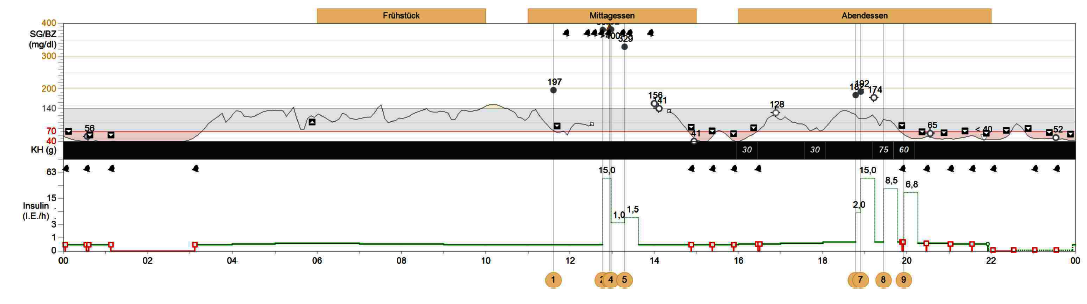
Abb. 2. Unterschiede zwischen der Blutglukose und der Glukose im Gewebe (CGM) gegen 19.00 Uhr. Beide Werte sind richtig. Die Unterschiede haben ihre Ursache in dem „Abfließen“ von Glukose aus dem Blut zur Auffüllung (Restauration) der Zuckerspeicher, die durch mehrfach wiederkehrende Unterzuckerungen geleert sind. Das ist ein Zustand großer Glukosedynamik.
Offensichtlich ist es nicht verkehrt, sich nach der Gewebeglukose zu orientieren. Das Blut ist das Transportsystem unter anderem für die Glukose (von der geringen Glukoseaufnahme in die Blutzellen einmal abgesehen).
Dagegen ist die Peripherie des Körpers das biologische System, in welchem die Stoffwechselvorgänge stattfinden. Die Blutglukose repräsentiert die Glukosekonzentration im Transportsystem, der CGM-Wert (Gewebeglukose) dagegen jene im biologischen System. Im Zustand normaler und geringer Glukosedynamik stimmen Blut- und Gewebeglukose überein, weshalb die Orientierung der Therapie anhand der Blutglukosewerte korrekt ist.
Im Zustand großer Glukosedynamik (Sport, Unterzuckerungen mit Gegenregulation, Pseudonormalisierung) stimmen die Glukosewerte im Blut und Gewebe jedoch nicht überein. Das ist biologisch bedingt und kein Messfehler.
Mittlerweile ist es auch üblich, die von den Glukosesensoren im Gewebe gemessenen Werte in der Therapie zu nutzen. Zum Teil werden die Werte mittels Rechenregeln zwar an die Blutglukosewerte angeglichen, aber auch Systeme die das nicht tun liefern eine gute Grundlage für die Überprüfung und Steuerung der Diabeteseinstellung.
Literatur
[1] Thomas A, Kolassa R, von Sengbusch S, Danne T. CGM interpretieren: Grundlagen, Technologie, Charakteristik und Konsequenzen des kontinuierlichen Glukosemonitorings. 2. Überarbeitete Auflage. Kirchheim-Verlag 2019; ISBN 978-3-87409-690-4. Seite
Siegmund T, Kolassa R, Heinemann L, Thomas A. Discrepancies Between Blood Glucose and Interstitial Glucose—Technological Artifacts or Physiology: Implications for Selection of the Appropriate Therapeutic Target. Journal of Diabetes Science and Technology 2017; 766-772.
