- Technik
EU-Behörde empfiehlt Zulassung für Glukagon-Nasenspray
2 Minuten
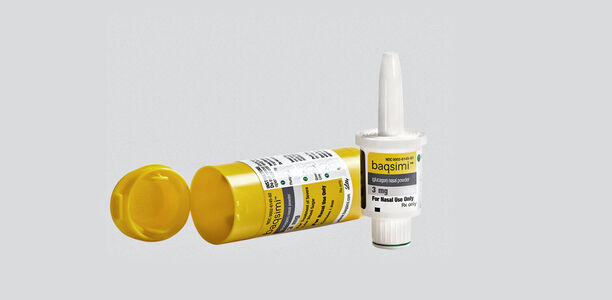
Kann ein Mensch mit Diabetes durch den Zustand einer schweren Unterzuckerung selbst nicht mehr gegen diese angehen, muss ihm Glukagon verabreicht werden. Bislang ist dies nur durch eine Injektion möglich. Nun wurde von der zuständigen EU-Behörde eine Zulassungsempfehlung für ein sofort gebrauchsfertiges Glukagon-Nasenspray abgegeben.
In der vergangenen Woche hat der Ausschuss für Humanarzneimittel (CHMP) der europäischen Arzneimittelbehörde (EMA) ein positives Gutachten verabschiedet, in dem die Zulassung eines sofort einsetzbaren Notfall-Glukagon-Nasensprays bei schweren Unterzuckerungen (Hypoglykämien) in der EU empfohlen wird. Die Zulassung in den USA durch die dortige Arzneimittelbehörde FDA wurde im Sommer erteilt und das Nasenspray ist dort bereits in Apotheken erhältlich.
Glukagon ist ein Hormon, das wie Insulin in der Bauchspeicheldrüse gebildet wird und als dessen Gegenspieler fungiert: Es erhöht die Blutzuckerkonzentration durch Stimulierung des Glykogenabbaus und Freisetzung von Glukose aus der Leber. Im Falle einer schweren Unterzuckerung, bei der die Betroffenen sich nicht mehr selbst helfen können (beispielsweise durch den Verzehr von Traubenzucker), sorgt die Gabe von Glukagon dafür, den Blutzuckerspiegel wieder in ausreichendem Maße zu erhöhen.
Die Zulassungsempfehlung gilt für Menschen mit Diabetes ab vier Jahren
Bislang gibt es ausschließlich Glukagon-Kits auf dem Markt, bei denen man vor dem Einsatz Glukagon in Pulverform mit einer Lösungsflüssigkeit vermischen muss, bevor die fertige Lösung mit einem Pen in eine Muskelpartie gespritzt wird.
Das neue nasale Glukagon liegt hingegen in einem gebrauchsfertigen Applikator für den einmaligen Gebrauch vor. Im Falle einer schweren Unterzuckerung können Helfende damit den Betroffenen das Glukagon-Spray über die Nase verabreichen, wo es über die Schleimhäute aufgenommen wird. Die Anwendung ist also so simpel wie bei anderen Nasensprays, beispielsweise solche gegen Heuschnupfen.
Die Zulassungsempfehlung der CHMP für das neue Glukagon-Nasenspray gilt für „die Behandlung von schwerer Hypoglykämie bei Erwachsenen, Jugendlichen und Kindern ab 4 Jahren mit Diabetes mellitus“. Es wurde vom Unternehmen Lilly entwickelt und wird unter dem Handelsnamen Baqsimi vertrieben. Auf Basis der Empfehlung wird die Europäische Kommission nun in naher Zukunft eine finale Entscheidung über die Zulassung treffen – erwartungsgemäß ist dies nach positivem CHMP-Bescheid eine reine Formsache.
Autor:
|
|
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Ähnliche Beiträge
- Behandlung

5 Minuten
- Behandlung
4 Minuten
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Geschichten, Gemeinschaft, Gesundheit: Der Diabetes-Anker ist das neue Angebot für alle Menschen mit Diabetes – live, gedruckt und digital. Der Diabetes-Anker und die Community sind immer da, wo du sie brauchst. Für alle Höhen und Tiefen.
über deinen Diabetes?
Die Antworten werden anonymisiert gesammelt und sind nicht mit dir oder deinem Profil verbunden. Achte darauf, dass deine Antwort auch keine Personenbezogenen Daten enthält.
-
anseaticids postete ein Update vor 6 Tagen, 18 Stunden
Wenn eine Diabetesdiagnose in eine Familie kommt, steht oft erst einmal alles Kopf.
Besonders für Kinder bedeutet sie eine enorme Veränderung und für Eltern die tägliche Sorge: „Wird mein Kind in der Kita oder Schule gut begleitet? Ist es sicher? Kann es trotz Diabetes unbeschwert Kind sein?“
Genau aus diesen Fragen heraus ist Hanseatic Kids entstanden: ein Herzensprojekt, das Kindern mit Diabetes im Alltag Sicherheit gibt und Familien entlastet.
Wir möchten dafür sorgen, dass kein Kind aufgrund seines Diabetes auf Ausflüge, Spielzeiten oder Schulaktivitäten verzichten muss. Unsere Begleiterinnen und Begleiter sind speziell geschult und unterstützen
individuell: beim Blutzuckermanagement, in Notfallsituationen, im Unterricht oder auf dem Pausenhof.So können Kinder lernen, wachsen und
selbstständig werden und Eltern wissen, dass ihr Kind gut aufgehoben ist.
Unsere Mission ist einfach:✔ Kindern Sicherheit geben
✔ Familien den Alltag erleichtern
✔ Kita- und Schulteams entlasten
✔ und vor allem: jedes Kind dabei unterstützen, frei und unbeschwert aufzuwachsen, trotz Diabetes.Gerade in den ersten Wochen nach der Diagnose oder wenn Unsicherheiten bestehen, sind wir an der Seite der Familien. Gemeinsam mit Eltern, Lehrkräften und Fachpersonal schaffen wir ein Umfeld, in dem Kinder sich wohlfühlen und ohne Angst lernen können.
Dieses Projekt ist für uns mehr als Arbeit, es ist eine Herzensangelegenheit. Jedes Kind hat das Recht auf Teilhabe, Freude und Freiheit. Wir möchten dazu beitragen, dass dies Wirklichkeit wird.
Wer mehr über unsere Arbeit erfahren oder Unterstützung anfragen möchte, kann sich jederzeit melden:
📧 moin@hanseatic-kids.de
📞 040 851 59 747 -
stephanie-bagehorn postete ein Update vor 1 Woche, 2 Tagen
Passend zu den kommenden Osterferien: Ein Backtipp für die ganze Familie: https://diabetes-anker.de/eltern-und-kind/wenn-diabetes-mit-im-osternest-liegt-gemeinsames-backen-mit-den-kindern/
Wenn Diabetes mit im Osternest liegt: gemeinsames Backen mit den Kindern – Diabetes-Anker
Ostern steht vor der Tür und im Gepäck sind viele süße Versuchungen. In diesem Zusammenhang stellt sich die Frage, wie zu starke Blutzucker-Anstiege bei Diabetes durch süßes Gebäck vermieden werden können. Selbst zu backen – erst recht gemeinsam mit den … Read more
-
othenbuehler postete ein Update vor 1 Woche, 3 Tagen
Viele Menschen mit Typ-1-Diabetes berichten, dass sich ihr Insulinbedarf im Verlauf des Menstruationszyklus verändert – oft deutlich spürbar, aber bisher kaum systematisch erfasst.
Genau hier setzt die TIMES-Studie an. Wir möchten besser verstehen, wie sich der Zyklus auf Glukosewerte und Insulinbedarf auswirkt – und wie Betroffene damit im Alltag umgehen.
👉 Wen suchen wir?
Personen mit Typ-1-Diabetes (18–40 Jahre), wohnhaft in Deutschland, mit regelmässigem Menstruationszyklus und Nutzung eines automatisierten Insulinabgabesystems.👉 Was bedeutet die Teilnahme?
Dauer: 6 Monate, bequem alles von zu Hause aus
Erfassung von Insulin-, Zyklus- und Aktivitätsdaten
Als Dankeschön: Clue-Abo (1 Jahr), Garmin-Uhr (zum Behalten) + Aufwandsentschädigung (siehe Flyer)Mit eurer Teilnahme helft ihr, Diabetes-Technologien zukünftig besser an zyklusbedingte Veränderungen anzupassen 💙
Mehr Infos im Flyer 👇













