- Behandlung
Insulin spritzen mit Insulinpens und -pumpen
6 Minuten

Welche Insuline gibt es? Welche Faktoren beeinflussen, wie Insulin wirkt? Welche Unterschiede gibt es zwischen vom Körper gebildetem und als Medikament gespritztem Insulin? In diesem Artikel gibt es Antworten.
Die Gabe von Insulin als Medikament ist für Menschen mit Typ-1-Diabetes lebensnotwendig. Für Menschen mit Typ-2-Diabetes ist Insulin eine Option neben weiteren möglichen Therapien. Die Insulininjektion erfolgt in das Unterhautfettgewebe (subkutan). Dadurch sind Eintritt und Dauer der Wirkung des Insulins anders als bei Insulin, das im Körper selbst gebildet und freigesetzt wird.
Insulin ist das wichtigste Hormon zur Regulation des Glukosestoffwechsels. Es sorgt dafür, dass Glukose aus dem Blut in die Zellen transportiert werden kann, also dorthin, wo sie zum Gewinnen von Energie genutzt wird. Dabei hängt die Wirkung von mehreren Faktoren ab, unter anderem davon, wie es im Körper verteilt wird. Der Hauptanteil des körpereigenen, von der Bauchspeicheldrüse abgegebenen Insulins gelangt über die Pfortader in die Leber (siehe Abbildung 1).
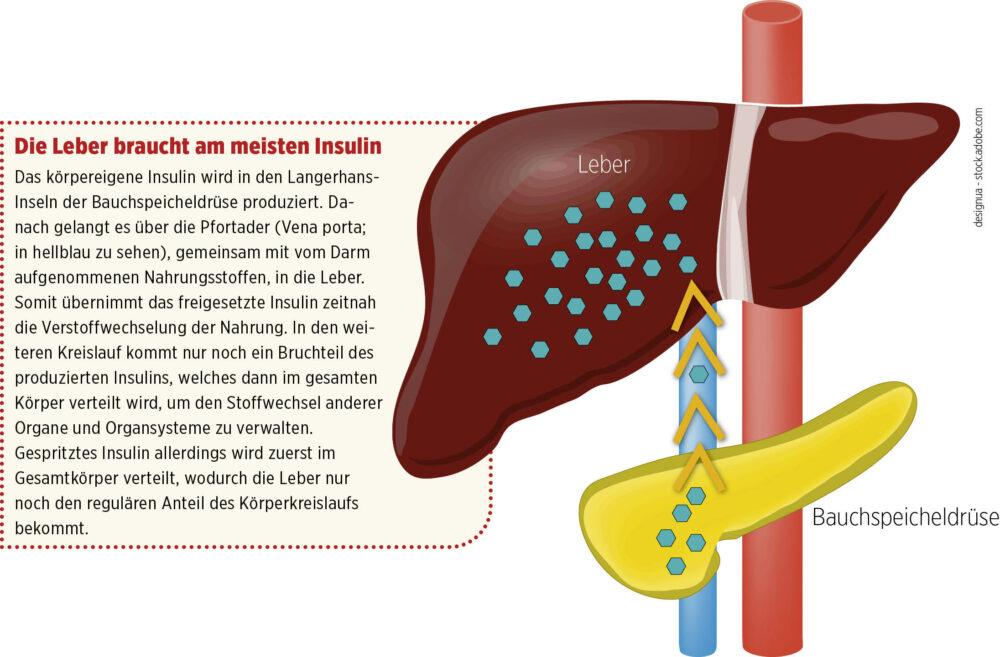
Abb. 1: Sekretion von Insulin über die Pfortader in die Leber.
Die Insulinkonzentration ist deshalb bei Menschen ohne Diabetes in der Leber deutlich höher als im übrigen Körper. Dieser Unterschied in der Konzentration geht jedoch verloren, wenn Menschen mit Diabetes Insulin subkutan spritzen. Die Leber baut normalerweise den größten Teil des von der Bauchspeicheldrüse abgegebenen Insulins ab. Bei injiziertem Insulin spielen die Nieren eine größere Rolle beim Abbau, da das Insulin nicht direkt in die Leber gelangt.
Wenn also Insulin auf subkutanem Weg als Medikament angewendet wird, kommt es zu einer von der normalen Wirkung des Insulins abweichenden Aufnahme und Verteilung (Pharmakokinetik) sowie Wirkung (Pharmakodynamik). Die Pharmakokinetik beschäftigt sich mit den Prozessen, welchen ein Medikament im Körper ausgesetzt ist: Aufnahme (Resorption, Absorption), Verteilung (Distribution), Verstoffwechselung (Metabolismus) und Ausscheidung (Exkretion, Elimination). Unter Pharmakodynamik versteht man die physiologischen, biochemischen und molekularen Auswirkungen des Medikaments auf den Körper.
Das Insulinmolekül
Insulin ist ein Eiweiß-Hormon (Peptid-Hormon), das aus einer Reihe von Aminosäuren besteht. Es liegt in einer Hexamer-Struktur vor, also einer Struktur aus sechs gleichartigen Insulin-Molekülen. Nach der Injektion spaltet sich diese Sechser-Struktur zuerst in Dimere (zwei Moleküle) und dann in Monomere (ein Molekül) auf. Die Insulin-Dimere und -Monomere können in die Blutgefäße aufgenommen werden (siehe Abbildung 2). Je schneller die Freisetzung von Insulin-Monomeren aus Hexameren ist, desto schneller gelangt das injizierte Insulin in den Blutkreislauf. Mit verschiedenen Hilfsstoffen in der Insulin-Lösung oder Veränderungen des Insulin-Moleküls kann dies beeinflusst werden.
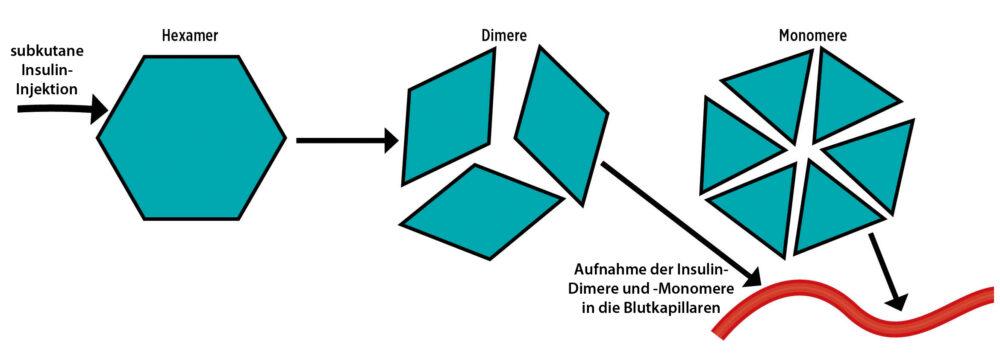
Abb. 2: Aufspaltung der Hexamer-Struktur eines Insulinmoleküls nach der Injektion. Je größer der Anteil von Dimeren und Monomeren ist, desto schneller ist die Aufnahme des Insulins in die Blutkapillaren. Mit verschiedenen Änderungen des Insulin-Moleküls (Insulinanaloga) kann die Geschwindigkeit der Freisetzung von Monomeren und Dimeren aus den Hexameren beeinflusst werden.
Unterschiedliche Arten von Insulin
Insulin-Präparate können aufgrund des Zeitpunkts des Wirkeintritts und der Dauer der pharmakologischen Wirkung in schnell-, kurz-, mittel- und langwirkende Insuline unterteilt werden. Die schnell- und kurzwirksamen Insulin-Präparate werden auch als prandiales Insulin bezeichnet, da sie zu den Mahlzeiten gespritzt werden, um den Anstieg der Glukosewerte durch Kohlenhydrate auszugleichen.
Die mittel- und langwirksamen Insulin-Präparate werden als Basalinsulin bezeichnet. Sie werden in der Regel nur ein- oder zweimal täglich gespritzt und dienen der Kontrolle des immer vorhandenen Grundumsatzes von Glukose, unabhängig von Mahlzeiten. Darüber hinaus sind einige Insulin-Produkte als Mischungen erhältlich, die sowohl einen prandialen als auch einen basalen Anteil besitzen. Eine Insulintherapie sollte idealerweise die Freisetzung von Insulin so genau wie möglich wie bei Menschen ohne Diabetes nachahmen.
Insulin-Arten
- Verschiedene Insulin-Arten können unterschiedlich schnell und lang wirken.
- Schnellwirkende Insuline werden bevorzugt zu Mahlzeiten angewendet. Die Wirkung tritt bereits nach wenigen Minuten auf und erreicht innerhalb von 1 – 2 Stunden einen Höhepunkt. Ab spätestens 5 Stunden gilt die gesamte Menge als vollkommen verstoffwechselt.
- Mittellang- und langwirksame Insuline werden eher für den ständig aktiven Stoffwechselbedarf gespritzt. Mittlerweile gibt es Langzeit-Insuline, deren Gesamtwirkdauer 24 Stunden überschreitet.
Schnell- und kurzwirkende Insuline
Die Aufnahme der Insulin-Moleküle ist, wie beschrieben, bei Monomeren am höchsten, gefolgt von Dimeren und Hexameren. Dieses Wissen wurde bei der gentechnischen Herstellung von Insulinanaloga eingesetzt, die in schnellwirkenden Insulin-Präparaten verwendet werden und nur geringfügige Unterschiede im Aufbau des Moleküls im Vergleich zum menschlichen Insulin aufweisen. Diese schnellwirkenden Insulinanaloga haben nach der Injektion ins Unterhautfettgewebe einen größeren Anteil an Monomeren.
Das Ergebnis ist eine schnellere Aufnahme ins Blut mit schnellerem Wirkeintritt, einer höheren maximalen Konzentration im Blut und einer kürzeren Wirkdauer im Vergleich zu Humaninsulin (siehe Abbildung 3). Die Wirkung tritt meistens innerhalb von etwa 15 Minuten ein. Um Blutzuckerspitzen nach den Mahlzeiten vorzubeugen, kann es deshalb sinnvoll sein, die Mahlzeitendosis bereits 15 bis 30 Minuten vor dem Start der Mahlzeit zu spritzen.
Mittel- und langwirksame Insuline
Im Gegensatz zu schnell- und kurzwirkenden Insulin-Präparaten werden mittellang- und langwirkende Präparate verzögert aufgenommen. Zu diesen Insulinen gehören NPH-Insuline und langwirkende Insulinanaloga:
NPH-Insulin
Das heute nur noch selten verwendete Insulin-Präparat mit Neutralem Protamin Hagedorn (NPH) enthält Humaninsulin als aktiven Wirkstoff. Durch die Bindung an das Protein NPH wird die Wirkung verzögert und verlängert. NPH-Insulin ist eine trübe Suspension und muss vor dem Spritzen geschwenkt bzw. gerollt werden, um es wieder zu vermischen. Erfolgt das unzureichend, kann die Wirkung schwanken.
Langwirkende Insulinanaloga
Durch Änderung der Reihenfolge der Aminosäuren des Insulin-Moleküls oder Anhängen von Fettsäuren können nicht nur schneller, sondern auch langsamer wirkende Insulin-Präparate hergestellt werden. Diese Veränderungen führen zu einer anhaltenden und langsamen Freisetzung von Insulin-Monomeren. Damit wird erreicht, dass bei täglicher Injektion etwa 24 Stunden lang Insulin im Körper zur Verfügung steht. Diese Insulinanaloga liegen in homogenen Lösungen vor, müssen also vor dem Spritzen nicht erst vermischt werden.
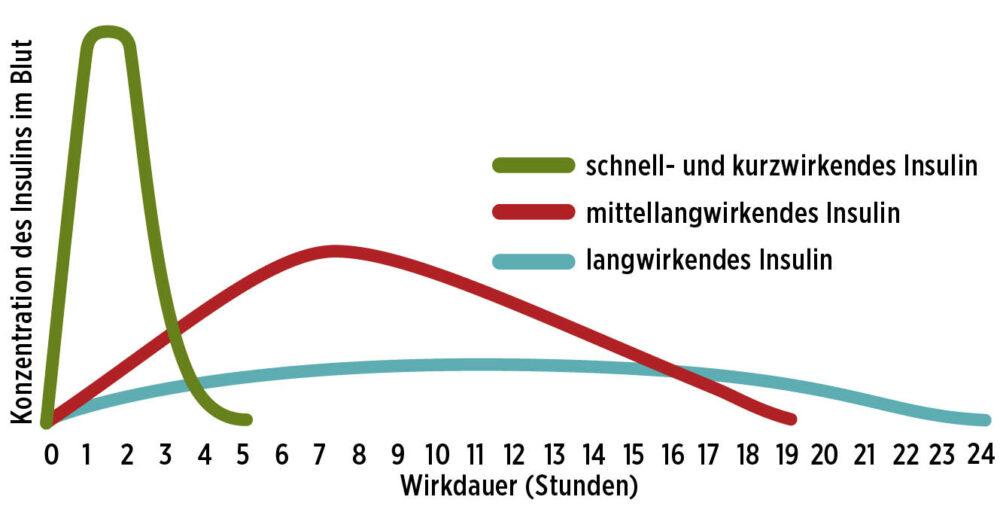
Abb. 3: Wirkungsschema verschiedener Insulin-Arten.
Insulingabe in das Unterhautfettgewebe
Das subkutane Gewebe (die Unterhaut) besteht hauptsächlich aus Fettzellen, die zu etwa 10 Prozent mit Fasern des Bindegewebes umgeben sind. Medikamente, die subkutan injiziert werden, können hier in Kapillargefäße des Blutkreislaufs aufgenommen werden.
Zur Injektion gibt es Insulinspritzen, Insulinpens oder Insulinpumpen. Die intensivierte Insulintherapie (ICT) wird hierzulande heute meist mit Insulinpens durchgeführt. Auch möglich ist die Therapie mit einer Insulinpumpe, bei der das Insulin über ein Infusionsset, bestehend aus einem Schlauchsystem und einer Kanüle, oder bei Patch-Pumpen direkt mit der integrierten Kanüle ins Unterhautfettgewebe gelangt. Um Veränderungen des Gewebes, wie Fettgewebe-Wucherungen (Lipohypertrophien) zu verhindern, ist eine saubere Injektionstechnik wichtig, mit Auswahl der richtigen Länge der Kanülen, regelmäßigem Wechsel der Injektionsstelle und nur einmaliger Nutzung der Kanüle.
Injektion des Insulins ins Subkutangewebe
Die Spitze der Kanüle von Spritze, Insulinpen oder -pumpe sollte weder in der äußersten Hautschicht verbleiben noch bis in die Muskelschicht gelangen. Der ideale Ort für die Aufnahme des verabreichten Insulins ist das Subkutangewebe.
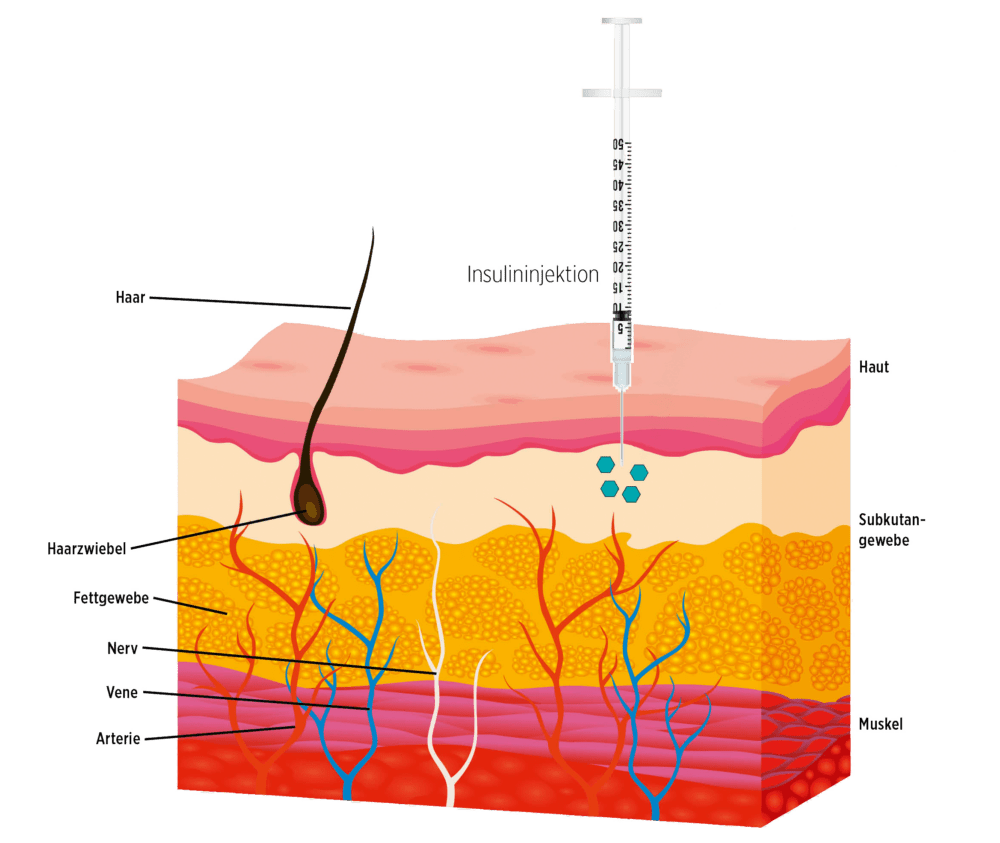
Nach Abgabe über Spritze, Insulinpen oder -pumpe kommt Insulin zuerst in der Zwischenzellflüssigkeit an und wird dann aufgespalten und über die Kapillargefäße (kleinste Gefäße des Körpers) in den Blutkreislauf aufgenommen und im Körper verteilt (s. auch Abb. 2).
Die Hautdicke ist an den üblichen Injektionsstellen, wie Bauch und Oberschenkel, bei allen Menschen ähnlich und beträgt etwa 2 Millimeter. Allerdings kann die Dicke des Unterhautfettgewebes je nach Body-Mass-Index, Geschlecht und Injektionsstelle deutlich unterschiedlich sein. Unabhängig von der Dicke des Unterhautfettgewebes macht die Einstichtiefe in Bezug auf die Aufnahme des gespritzten Insulins keinen besonderen Unterschied, es sei denn, die Injektion erfolgt in die darunterliegende Muskulatur. Letzteres führt zur schnelleren Aufnahme in den Blutkreislauf und somit zu einer veränderten Pharmakokinetik und Pharmakodynamik. Es ist also wichtig, die Länge der Kanüle passend auszuwählen, um einen zu tiefen Einstich zu vermeiden.
Variabilität des Unterhautfettgewebes
Auch andere Faktoren wie das Alter, Störungen des Wasserhaushalts, verschiedene Krankheiten oder Einlagerungen von Wasser (Ödeme) in verschiedenen Körperregionen können einen Einfluss auf die Pharmakokinetik und Pharmakodynamik von gespritztem Insulin zeigen.
Zusammenfassung und Fazit für die Praxis
Aus pharmakokinetischer und pharmakodynamischer Hinsicht bestehen wichtige Unterschiede zwischen dem körpereigenen und dem als Medikament eingesetzten Insulin. Bei einer Insulintherapie ist es wichtig, über die Wirkprofile und die Injektionstechnik aufgeklärt zu sein. Aufmerksamkeit sollte dabei auf die Einstichstelle gelegt werden, da die häufige bzw. dauerhafte Injektion des Insulins in dieselbe Region zu Änderungen der Gewebestruktur führen kann.
Schwerpunkt: Wie Insulin entsteht und funktioniert
- So entsteht und wirkt Insulin im Körper
- Insulin spritzen mit Insulinpens und -pumpen
- Langzeit-Insuline können die Therapie verändern
von Dr. Guido Freckmann, Sükrü Öter, Dr. Delia Waldenmaier, Dr. Sandra Schlüter
Erschienen in: Diabetes-Anker, 2024; 72 (5) Seite 20-23
Diabetes-Anker-Newsletter
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Ähnliche Beiträge
- Ernährung
Rezept für Lachs-Spieße mit Zitronen-Kräuter-Dip

2 Minuten
- Eltern und Kind
Serie – AID-Systeme für Kinder und Jugendliche: automatisierte Insulinabgabe ohne Schlauch mit Omnipod 5

4 Minuten
Keine Kommentare
Über uns
Geschichten, Gemeinschaft, Gesundheit: Der Diabetes-Anker ist das neue Angebot für alle Menschen mit Diabetes – live, gedruckt und digital. Der Diabetes-Anker und die Community sind immer da, wo du sie brauchst. Für alle Höhen und Tiefen.
Diabetes-Anker-Newsletter
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Anzeige
Recor Medical
Das Verfahren der renalen Denervierung kann helfen, den Blutdruck effektiv zu senken.

