- Behandlung
So entsteht und wirkt Insulin im Körper
6 Minuten
Mit der Entdeckung des Insulins 1921 durch Frederick Banting und Charles Best begann die Erforschung dieses lebenswichtigen Hormons als zentraler Faktor zahlreicher hormoneller Regelkreise. Das Ziel aus nun über 100 Jahren Insulinforschung bestand und besteht darin, aufzuklären, wo überall und wie Insulin genau im Körper wirkt.
So soll die Therapie mit Insulin für Menschen mit Diabetes mellitus immer weiter an die natürliche Wirkkurve und Wirkweise des aus den Beta-Zellen der Bauchspeicheldrüse direkt in die Blutbahn freigesetzten Insulins angepasst werden.
Nachdem Forschende verstanden hatten, wie Insulin im Körper freigesetzt wird und wirkt, konnten sie die modernen lang und kurz wirkenden Insulinanaloga entwickeln. Mit diesen modernen Molekülen, die Insulin nachahmen, kann ins Unterhautfettgewebe, also subkutan, gespritztes Insulin immer besser wie natürlich im Körper, also endogen, gebildetes Insulin wirken.
Auch wenn man in den letzten Jahren entscheidende Fortschritte in der Insulintherapie erreichen konnte, bleiben dennoch viele Herausforderungen in der Insulintherapie offen. Die Zukunft liegt in der Entwicklung von Insulinen mit weiter der natürlichen Wirkkurve angepassten Substanzen, die auf die Glukosewerte im Körper reagieren und die sich wie endogenes Insulin verteilen und auch so wirken.
Regulation der Glukosewerte
Während verschiedene im menschlichen Körper gebildete Hormone wie Glukagon, Stresshormone, Wachstumshormon oder Kortison Blutzucker steigern, ist Insulin das einzige Hormon im menschlichen Körper, das die Glukosewerte senkt. Wird die Bildung oder Wirkung von Insulin beeinträchtigt, ist das zwangsläufig mit einem Anstieg der Glukosewerte und dem Entstehen eines Diabetes mellitus verknüpft.
Die wichtigste Rolle in der Regulation der Glukosekonzentration kommt den Langerhans-Inseln in der Bauchspeicheldrüse, dem Pankreas, zu. Die Langerhans-Inseln bestehen aus vier unterschiedlichen Zelltypen:
Als wichtigste Regulatoren der Glukosekonzentration sind die beiden hormonellen Gegenspieler Insulin und Glukagon anzusehen. Wie in der folgenden Abb. 1 dargestellt, führt dabei ein Anstieg der Glukosekonzentration (Hyperglykämie) zu einer vermehrten Ausschüttung von Insulin aus den Beta-Zellen und einer verminderten Freisetzung von Glukagon aus den Alpha-Zellen. Umgekehrt führt eine niedrige Glukosekonzentration (Hypoglykämie) zu einer vermehrten Freisetzung von Glukagon aus den Alpha-Zellen und einer reduzierten Freisetzung von Insulin aus den Beta-Zellen. Bei Menschen ohne Diabetes wird über diesen Kontrollmechanismus die Glukosekonzentration im Blut in einem Bereich von etwa 60 bis 160 mg/dl (3,3 – 8,9 mmol/l) sehr stabil gehalten.
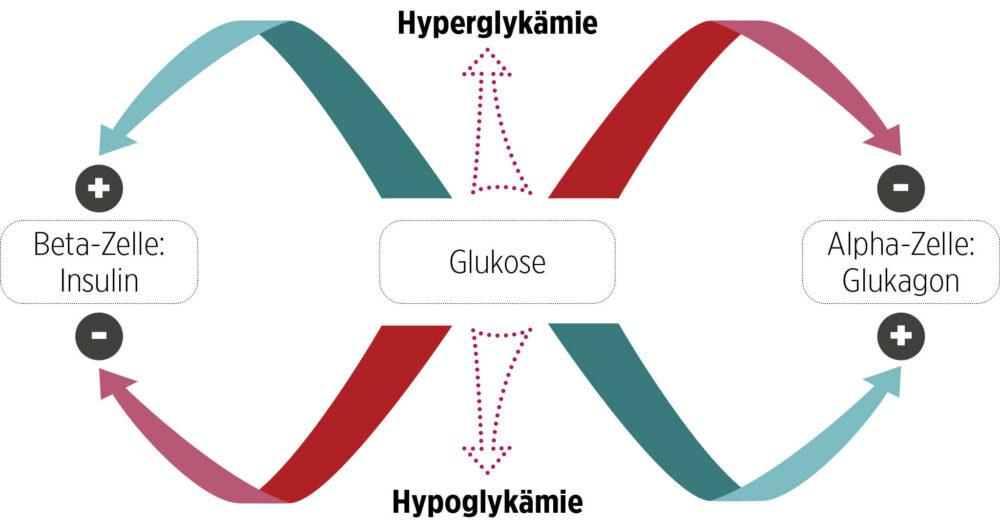
Abb. 1: Schema des Glukosestoffwechsels.
Neben den glukosesenkenden Eigenschaften des Insulins haben Forschende zwischenzeitlich auch weitere Effekte des Insulins erkannt und in ihrer Bedeutung neu eingestuft. Auch wenn die Bedeutung des Insulins für eine normale, physiologische Regulation des Glukosestoffwechsels essenziell ist, werden ihm weitere Eigenschaften in der Regulation der Nahrungsaufnahme, des Fettstoffwechsels, der Stimulation von Wachstumsprozessen und Regulationen im Herz-Kreislauf-System zugeschrieben. Von Glukose unabhängige Wirkungen des Insulins konnten in unterschiedlichsten Geweben gezeigt werden. Etwa dem Gehirn, dem Herzen, den Nieren, den Knochen, dem Fettgewebe, der Haut und den Haarfollikeln.
So wird Insulin in der Beta-Zelle gebildet
Auch wenn nach neueren Forschungsergebnissen Insulin auch in bestimmten Regionen des zentralen Nervensystems zu finden ist, stammt der wesentliche Anteil des im Körper vorkommenden Insulins aus den Beta-Zellen der Langerhans-Inseln in der Bauchspeicheldrüse. Insulin ist ein Eiweiß (Peptid), welches aus 51 Aminosäuren besteht. Diese sind in zwei Ketten angeordnet, einer A-Kette mit 21 Aminosäuren und einer B-Kette mit 30 Aminosäuren. Beide Ketten werden durch zwei Schwefelbrücken (Disulfidbrücken) verbunden. Bei Menschen liegt der Code für die Reihenfolge der Aminosäuren des Insulins auf dem Chromosom 11.
Bei der Synthese des Insulins sind einige Strukturen in den Zellen beteiligt. Zunächst wird eine Vorstufe des Insulins, das Präproinsulin, in den Ribosomen der Beta-Zelle gebildet. Nach Abspaltung von 23 Aminosäuren im endoplasmatischen Retikulum in der Zelle entsteht Proinsulin mit 86 Aminosäuren. Proinsulin wird im Anschluss in den Golgi-Apparat der Beta-Zellen transportiert und dort durch Enzyme in zwei Teile gespalten: das finale Insulin und ein weiteres, als C-Peptid (Connecting Peptide) bezeichnetes Eiweiß. Beide Peptide werden anschließend in die Blutbahn freigesetzt. Sie erreichen mit dem Blutstrom dann die Zielzellen in den verschiedenen Geweben des Körpers.
Wie die Freisetzung von Insulin aus der Beta-Zelle erfolgt
Das Freisetzen von Insulin aus der Beta-Zelle erfolgt dabei in strenger Abhängigkeit von der Glukosekonzentration. Es kann in zwei Phasen unterteilt werden (siehe Abbildung 2): eine erste, nur wenige Minuten anhaltende Phase, die sofort nach einem Glukoseanstieg durch Freisetzung von in der Beta-Zelle bereitliegenden insulinhaltigen Betagranula aus der Beta-Zelle erfolgt.
Die zweite über Stunden andauernde Phase wird durch die Dauer der Glukoseerhöhung getriggert und im Wesentlichen von neu gebildetem Insulin gespeist. Bei Glukosekonzentrationen unter 90 mg/dl (5,0 mmol/l) wird kein Insulin mehr aus der Beta-Zelle in die Blutbahn freigesetzt.
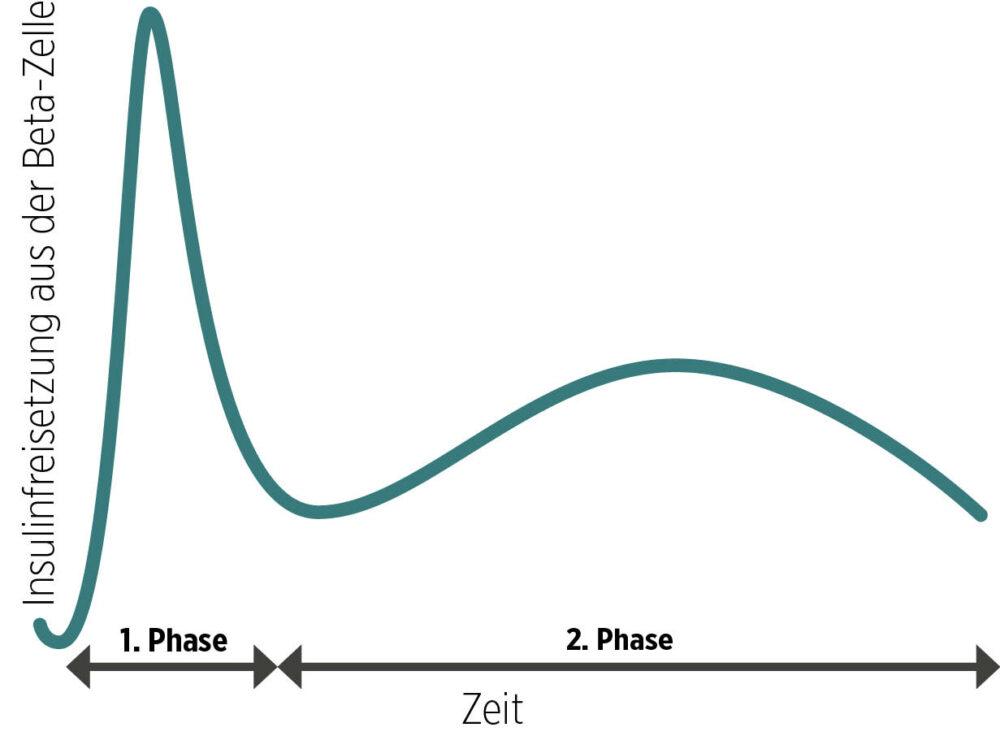
Abb. 2: Schema der Freisetzung von Insulin aus der Beta-Zelle.
Die Synthese und insbesondere die Freisetzung des Insulins aus der Beta-Zelle unterliegt, wie gesagt, primär der Glukosekonzentration. Steigt z.B. nach einer kohlenhydrathaltigen Mahlzeit die Glukosekonzentration in der Gewebeflüssigkeit, die die Beta-Zelle umgibt, an, wird vermehrt Insulin aus der Beta-Zelle freigesetzt. Darüber hinaus können verschiedene nervliche und hormonelle Einflüsse die Insulinfreisetzung aus der Beta-Zelle maßgeblich beeinflussen. So kann beispielsweise die Freisetzung bestimmter Hormone aus dem Darm nach einer Mahlzeit die aus den Beta-Zellen abgegebene Insulinmenge deutlich steigern. Diese Darmhormone, auch als Inkretine bezeichnet, spielen eine wichtige Rolle bei der Kontrolle der Blutzuckeranstiege nach einer Mahlzeit.
So wirkt Insulin im Körper
Nach Freisetzung des Insulins aus der Beta-Zelle erreicht es zunächst mit dem Blutstrom über die Pfortader die Leber. Dort hemmt es die Freisetzung von Glukose aus der Leber in die Blutbahn. Dies ist insbesondere nach kohlenhydrathaltigen Mahlzeiten wichtig und verhindert übermäßige Glukoseanstiege nach dem Essen. Wenn das Insulin durch die Leber strömt, wird bereits ein Großteil des Insulins abgebaut. Dadurch ist die Insulinkonzentration in Geweben außerhalb des Körperstamms (in den peripheren Geweben) deutlich niedriger als in der Leber. Man spricht hier auch von einem hepato-peripheren Insulinquotienten.
Nachdem das Insulin die Leber verlassen hat, gelangt es in die Peripherie des Körpers. Dort ermöglicht es die Glukoseaufnahme in Muskel- und Fettzellen. Während Leber-, Muskel- und Fettzellen Glukose nur mithilfe des Insulins aufnehmen können, sind andere Gewebe wie Gehirn, rote Blutkörperchen, Nervenzellen oder die Niere in der Lage, Glukose auch ohne die Hilfe von Insulin in die Zellen aufzunehmen.
Insulin wirkt über einen Insulinrezeptor
Insulin entfaltet seine biologische Aktivität über Rezeptoren an der Wand der Zelle, der Zellmembran. Nach Bindung des Insulins an den Rezeptor wird dieser aktiviert und es werden unterschiedliche Signalwege in der Zelle angestoßen. Über diese Signalwege werden in den Zellen die für diese Zellen spezifischen Effekte des Insulins ausgelöst. So führt die Aktivierung des Insulinrezeptors in den peripheren Muskel- und Fettzellen zur Aktivierung von Glukosetransportern in der Zellwand und damit zur Aufnahme der Glukosemoleküle in Muskel- und Fettzellen.
Nach der Aufnahme der Glukose in die Zielzellen wird diese entweder in Energie umgewandelt oder gespeichert als Glykogen. Diesen Speicher nutzt der Körper später zum Gewinnen von Energie. In der Zelle kann die Glukose auch in Fette umgewandelt werden. Diese Triglyzeride stehen ebenfalls als Reserve für ein späteres Gewinnen von Energie zur Verfügung.
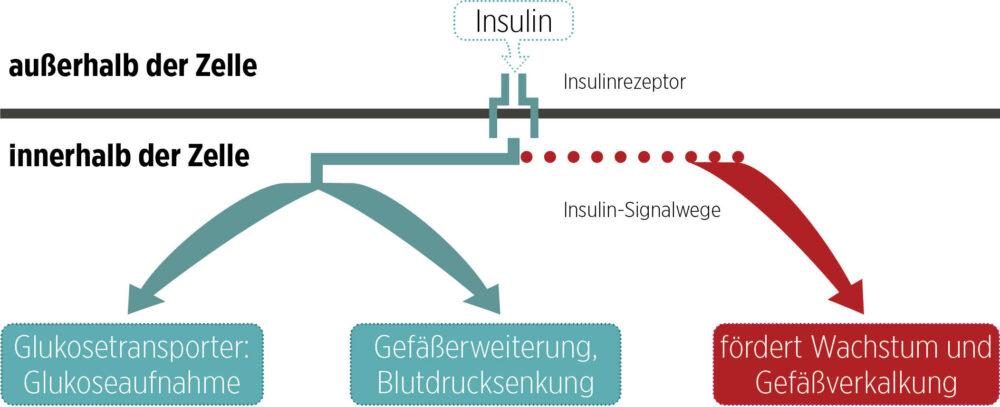
Abb. 3: Effekte der Aktivierung des Insulinrezeptors in unterschiedlichen Zelltypen.
Wie in der Abbildung 3 dargestellt, kann die Aktivierung des Insulinrezeptors in anderen Zellen noch ganz andere Effekte haben. So führt die Aktivierung des Insulinrezeptors in Gefäßzellen (Endothelzellen) bspw. zu einer Erweiterung der Gefäße und damit einem Sinken des Blutdrucks. Andere durch Insulin ausgelöste Signalwege können Wachstumsprozesse aktivieren oder beispielsweise im Knochengewebe zur Aktivierung knochenbildender Zellen führen.
Zusammenfassung
Zusammenfassend handelt es sich beim Hormon Insulin um ein lebenswichtiges Hormon, welches eine zentrale und komplexe Rolle in der Regulation des Glukose-, Fett- und Energiehaushalts spielt. Die Bildung und Freisetzung des Hormons unterliegt primär der Glukosekonzentration außerhalb der Zellen. Es wird aber durch andere hormonelle und nervliche Signale maßgeblich beeinflusst. Störungen in der Bildung oder Wirkung von Insulin sind häufig mit der Entwicklung eines Diabetes mellitus verknüpft.
Neben diesen Wirkungen kommt Insulin auch außerhalb von Stoffwechselprozessen eine Rolle in der Regulation zahlreicher Signalwege und Wachstumsprozesse zu. Das Erforschen der Rolle des Insulins in den verschiedensten biologischen Regulationsprozessen ist ganz entscheidend, um Folgen krankhafter Störungen der Insulinbildung, -freisetzung und -wirkung mit neuen effektiven Medikamenten entgegentreten zu können.
Schwerpunkt: „Wie Insulin entsteht und funktioniert“
- So entsteht und wirkt Insulin im Körper
- Insulin spritzen mit Insulinpens und -pumpen
- Langzeit-Insuline können die Therapie verändern
Erschienen in: Diabetes-Journal, 2024; 73 (5) Seite 16-19
Diabetes-Anker-Newsletter
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Ähnliche Beiträge
- Aktuelles
Diabetes-Anker-Podcast – Höhen & Tiefen: Stephan Seiler – vom stillen Kämpfer zum Podcast-Host

2 Minuten
- Eltern und Kind
Kohlenhydrat-Apps im Überblick: Unterstützung für Diabetes-Management im Alltag

3 Minuten
Keine Kommentare
Diabetes-Anker-Newsletter
Alle wichtigen Infos und Events für Menschen mit Diabetes – kostenlos und direkt in deinem Postfach. Mit unserem Newsletter verpasst du nichts mehr.
Über uns
Geschichten, Gemeinschaft, Gesundheit: Der Diabetes-Anker ist das neue Angebot für alle Menschen mit Diabetes – live, gedruckt und digital. Der Diabetes-Anker und die Community sind immer da, wo du sie brauchst. Für alle Höhen und Tiefen.
Community-Frage
Mit wem redest du
über deinen Diabetes?
Die Antworten werden anonymisiert gesammelt und sind nicht mit dir oder deinem Profil verbunden. Achte darauf, dass deine Antwort auch keine Personenbezogenen Daten enthält.
Werde Teil unserer Community
Community-Feed
-
moira postete ein Update vor 2 Wochen, 3 Tagen
Ich hatte am letzten Wochenende viel Spaß mit Bluetooth: meine Pumpe und mein Handy wollten sich 1Stunde lang nicht koppeln – bis mein Mann auf die Idee kam es könnte an den 3 Bluetooth Controllern liegen mit denen gerade im selben Raum gespielt wurde. Mit genug Abstand klappte alles wieder hervorragend. 🙄
-
bloodychaos postete ein Update vor 3 Wochen, 3 Tagen
Hat noch jemand Probleme mit dem Dexcom G7? Nachdem ich letztes Jahr im Sommer über drei Monate massive Probleme mit dem G7 hatte bin ich zum G6 zurückgewechselt. Jetzt zum Jahreswechsel bzw. jetzt Ende Februar wollte ich dem G7 mal wieder eine Change geben. Ich war davon ausgegangen, dass die Produktionsprobleme inzwischen behoben sind. Aber spätestens am dritten Tag habe ich massive Abweichungen von 50 – 70 mg/dL. Setzstellenunabhängig. Meine aktuellen G7 wurden im Dezember 2025 produziert. Also sollten die bekannten Probleme längst behoben worden sein. Zuerst lief es die ersten Monate von 2025 mit dem G7 super, aber im Frühjahr 2025 fingen dann die Probleme an und seitdem läuft der G7 nicht mehr bei mir, obwohl alle sagen, dass die Probleme längst behoben seien und der Sensor so toll funktioniert. Ich habe echt Angst. Mir schlägt das sehr auf die Psyche. Zumal ich die TSlim nutze, die nur mit Dexcom kompatibel ist und selbst wenn ich zur Ypsopump wechsel ist da der Druck, dass es mit dem Libre3 funktionieren MUSS. Ich verstehe nicht, warum der G7 bei allen so super läuft, nur ich bin die Komische, bei der er nicht funktioniert.
-
ole-t1 antwortete vor 3 Wochen, 1 Tag
Kleine Ergänzung zum MeetUp von gestern.
Wenn ein “klassischer” Pumpenbetrieb ohne AID/Loop eine Option ist, dann tut sich eine breite Auswahl an CGM auf, die momentan auf dem deutschen Markt verfügbar sind:
Freestyle Libre 3 bzw. 3+
Dexcom G7
Dexcom G6 (noch)
Medtronic Guardian 4 (nur mit Medtronic-Pumpe)
Medtronic Simplera (nur mit Medtronic-Pumpe oder -Smartpen)
Eversense (implantiert für 1/2 Jahr, wird oft bei Pflasterallergien genutzt)
Accu-Chek Smartguide CGM
Medtrum Touchcare Nano CGMIch würde schätzen, dass die Reihenfolge ungefähr den Verbreitungsgrad widerspiegelt. Von Medtrum würde ich mir z.B. keinen grandiosen Kundenservice erhoffen. Aber wer weiß…?
Mag sein, dass ich etwas vergessen habe, aber die wichtigesten müssten dabei sein.
-
-
thomas55 postete ein Update vor 4 Wochen
Hallo,
ich habe zur Zeit die Medtronic Minimed 670G mit Libre als Sensor. Ich überlege, auf die 780G als AID mit dem Simplera umzusteigen. Hat jemand Erfahrung mit diesem Sensor? Wie sieht es mit der Verfügbarkeit aus? In der Vergangenheit wurden Neukunden der 780G nicht mit dem Simplera beliefert sondern nur Kunden, die die 780G schon länger nutzen. Das hat sich nach Aussagen von Medtronic-Mitarbeitern beim T1day heute genau umgekehrt. Mein Doc hat das vestätigt. Für mich als neuer Bezieher der 780G gut, für die Bestandskunden schlecht.
Danke vorab und bleibt gesund (von unserem Typ 1 lassen wir uns das Leben dank Technik nicht vermiesen!)
Thomas55-
crismo antwortete vor 4 Tagen, 21 Stunden
Hi Thomas 🙂
Ja genau für Bestandskunden bekommt man den Simplera leider nicht. Ich habe / hatte jetzt 8 Jahre lang die Pumpen von Medtronic. Aktuell hab ich die 780g noch bis Ende März, dann Wechsel ich zur Ypsopumpe.
Ich war eigentlich immer zufrieden mit der Pumpe und den Sensoren. Doch seit gefühlt einem Jahr sind die Guardian 4 Sensoren so schlecht geworden. Ich war dauerhaft damit beschäftigt, einen Sensor nach dem anderen zu reklamieren. Die Sensoren hielten bei mir nur max. 4-5 Tage. Danach war Schluss. Verschiedene Setzstellen wurden getestet, auch der Transmitter wurde getauscht. Aber es half alles nichts.Jetzt werde ich wechseln. Den Simplera wollte ich dann einfach nicht noch länger abwarten. Denn Bestandskunden hatten da leider das nachsehen. Schade Medtronic!!!
-
thomas55 antwortete vor 4 Tagen, 20 Stunden
@crismo: Ich habe mich nun auch für die Ypsopump entschieden. Ich wollte von medtronic Angebote für die 780 und den Simplera haben für die Krankenkasse zur Übernahme der Kosten. Ausserdem wollte ich eine Zusicherung haben, dass ich den Simplera überhaupt bekomme. Nach einer Woche kam das Angebot für die 780 per Post, von einem Angebot für den Simplera kein Wort. Ich bin privat versichert und muss an medtronic zahlen und dann eine Erstattung von der Krankenkasse beantragen. Weil der Simplera mehr als das Doppelte vom Libre kostet, wollte ich das der Krankenkasse vorher offenlegen. Dann habe ich eine Mail an medtronic geschrieben, nach 2 Wochen keine Reaktion. Dann habe ich mich für die Ypsopump entschieden. Das Angebot kam am nächsten Tag per Mail. Das ist für mich Service! Jetzt warte ich auf Zustimmung der Krankenkasse und dann Tschüss medtronic. Schade, ich finde die Pumpen (seit 12 Jahren genutzt) gut.
-









